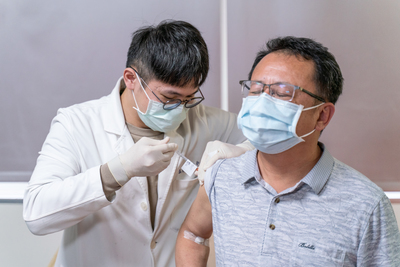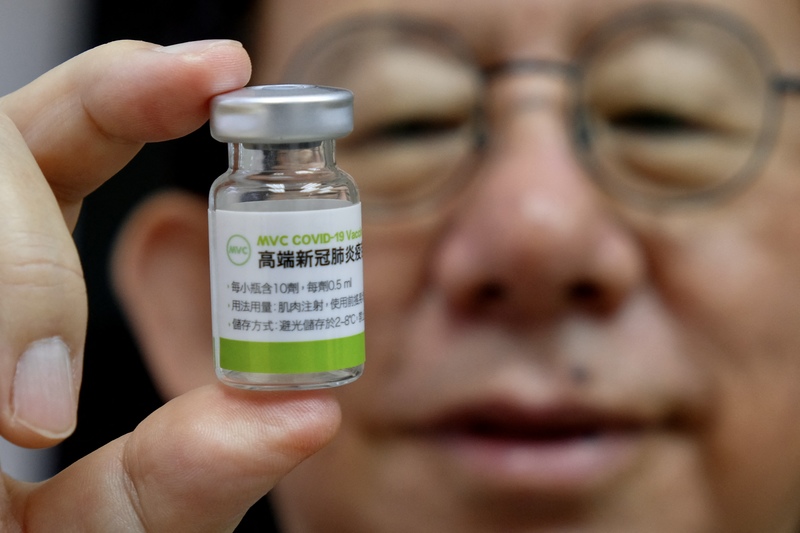
儘管風波不斷,台灣通過了第一支獲得緊急授權(Emergency Use Authorization, EUA)的國產疫苗。食藥署今(19)日在中央流行疫情指揮中心例行的防疫記者會中宣布,高端疫苗(MVC-COV1901)中和抗體數據不劣於AZ疫苗的中和抗體,得以專案製造申請案。高端的EUA審查會議於昨(18)日進行,最終20人投票,18人同意、1人不同意、1人主張補件,壓倒性通過,建議可提供20歲以上成人接種。
衛福部長陳時中坦言,高端的產量較小,將確認高端疫苗儲備量與生產量後,交由傳染病防治諮詢會預防接種組(ACIP)決定接種計畫。不過,審查會議過程沒有全程錄影,今天也未公布討論過程與細項指標。《報導者》採訪病毒學、感染症、公衛、臨床醫學等各領域專家,為讀者解析第一支國產疫苗EUA通過後,突破與創新、角色定位及法規和國際接軌上還將面對的挑戰。
食藥署署長吳秀梅指出,昨日邀請國內化學製造管制、藥學、毒理學、臨床醫學、公衛、法律及醫學倫理專家召開會議,討論高端疫苗專案製造申請案,經過一天充分討論,檢視高端疫苗中和抗體數據,不劣於AZ疫苗的中和抗體結果,達成食藥署公告「新冠疫苗專案製造或輸入技術性資料審查基準」要求,且安全性數據顯示無重大安全疑慮,在專家會議多數同意下,正式核准高端疫苗的專案製造。至於另一家聯亞疫苗,食藥署也已收到送件資料,但尚未確定審查會議日期。
今日指揮中心火速公布審查結果,不過,細部指標及審查內容都未公開,記者會也沒有計畫主持人或會議主席列席說明。陳時中說明,了解外界關心AZ中和抗體的實驗室結果,由於另一家疫苗聯亞正在申請EUA當中,聯亞也需要與AZ中和抗體進行比較,得不低於AZ中和抗體才能通過,在聯亞尚未審查前,將不公布AZ數據,避免出現不公平的狀況。
陳時中也解釋,對於審查過程有一派是主張全程公開,另一派是認為應該讓委員有表意權的自由,兩種意見沒有特別好或特別壞,等到兩家疫苗都審查完畢,自然會公布資料,「這些事情等兩家疫苗計畫都通過之後再說。」
食藥署於6月10日才公布EUA療效評估標準,是以免疫橋接方式,採用中和抗體效價作為替代療效指標,誘發的免疫原性不得低於AZ疫苗。高端今天隨即發出新聞稿表示,仍將進行第三期臨床試驗及其他驗證性試驗(如年齡層擴充),以取得常規藥證及國際認證為目標。
委員票數:扣除主席不參與投票,總計20名委員投票,18人同意、1人補件再議、1人不同意。
與AZ比較的結果:
- 原型株活病毒中和抗體幾何平均效價比值(geometric mean titer ratio, GMTR)95%信賴區間下限為3.4倍,大於標準要求0.67倍。
- 血清反應比率(sero-response rate)的95%信賴區間下限為95.5%,大於標準要求50%。
附帶條件:一年內檢送國內外執行疫苗保護效益(effectiveness)報告,以保障安全。
適用法源:食藥署依《藥事法》第48條之2規定,核准專案製造。
適用對象:20歲以上成人,接種兩劑,間隔28天。
不過今日EUA結果,因為沒有具體細部數據,相當於只公布了「一半」,加上產量問題,國產疫苗拿到EUA後,將在當下防疫上扮演什麼角色?這次爭議不斷的審查作業過程,台灣應有什麼思考與未來生技發展的考量?
以下是我們採訪不同領域專家的看法,以第一人稱表述。
施信如(長庚大學新興病毒感染研究中心主任):
指揮中心今天公布的「高端疫苗組與AZ疫苗組中和抗體幾何平均效價比值是下限的3.4倍」,這樣的說法不代表高端疫苗就比AZ疫苗保護力好3倍,這兩種疫苗的平台完全不同,這只是其中一個數據,不能這樣下定論。
按照實驗室數據,不管是國外的血清、還是近期國內的數據,指揮中心應該可以公布AZ的中和抗體數值的,因為接下來國際上也有很多論文會產出,這並不是祕密,數值愈不公開,猜測就愈多。目前國際中和抗體數值來看,莫德納約為1300、輝瑞約為950,AZ差異較大,約在150~500之間,而高端雖然之前中和抗體633,但國際標準計算下約為400左右。高端比mRNA疫苗低、跟AZ相比是差不多的。
今天通過高端疫苗的EUA,我認為是有好有壞的。從科學角度來看,高端沒有mRNA疫苗好,但也沒有到太差。高端所屬的蛋白疫苗副作用低,對有些無法接種mRNA、腺病毒疫苗的人,這確實可以提供一個選擇:抗體不到最高,但有保護效果,較無副作用,這對台灣民眾是好事。
現況台灣尚未有足夠疫苗,如果今天有千萬劑莫德納、BNT,就不用煩惱了。在仍缺乏疫苗的情況下讓國產疫苗通過EUA,也引起各界的疑慮,因為它並沒有正常地走完一、二、三期試驗,過程中包括疫苗平台不同、科學比較根據上也都有不足,如今出現一些對疫苗的負面看法。但能在讓「民眾有更多選擇」上,我相信還是一件好事。
不過不是緊急授權完就沒問題,接下來還是必須要求廠商在期限內做完三期試驗,明確表達要何時開始做、在哪裡做、收案數目多少,就算受到環境影響,可能不如預期收得多,也要實際執行,後續接種後的監測也要做好。

何美鄉(中研院生物醫學科學研究所兼任研究員):
目前國際通過的疫苗都是創新技術的mRNA與腺病毒載體,不管是因為醫學因素或心理因素不想打的人,通過蛋白質疫苗是多一種選擇。
EUA是因為使用者有迫切的需要,所以經過審查後通過讓大眾使用,這不是為了配合廠商的需要給它緊急授權。
目前國際上對於「未進行三期臨床試驗,以中和抗體做免疫橋接,中和抗體需要多少才具有充分的保護力?」這件事目前還沒有一個定論,我們國產疫苗使用比較AZ的方式做標準,學理上是可行,但實際上的保護力怎麼樣,仍必須驗證。緊急授權終究只是在防疫的節骨眼上不得不的做法,學界與公部門都有責任,必須在施打後收集更多資料,設計一些追蹤方法,來追蹤這款疫苗的真實效益。
過去蛋白質疫苗都是接種三劑為主,才能產生足夠保護力,像HPV(人類乳突病毒疫苗、即俗稱子宮頸癌疫苗)疫苗就是打三劑。所以,食藥署通過廠商的EUA後,之後怎麼要求廠商繼續往下做研究?追蹤研究怎麼開展?這些比較重要。我是會相信食藥署該做的都做了,但還是必須向民眾說明未來要怎麼做。
這次國產疫苗EUA標準,是以今年3月第一批AZ疫苗在國內接種時,桃園醫院蒐集200名接種者的中和抗體做比較。一般而言,拿新疫苗和已上市國際廠牌疫苗PK的方式,若新疫苗的抗體濃度相近、或優於已上市疫苗,則可視為具有保護力,被稱為「非劣性試驗」(non-inferiority trials)。
台灣大學農藝學系名譽教授、生物統計博士劉仁沛解釋,「非劣」的意思是比較概念,新的疫苗要達到多少效力,才能不劣於原先已上市的疫苗,並且獲得上市的資格。非劣性試驗評估的指標,跟一般常規三期試驗的指標類似,只是目的不同。常規三期試驗是要比安慰劑好;非劣性比較要證明疫苗效力不比選定對照的疫苗來得差,但比較過程中,評估的安全性、有效性、納入、排除指標的條件⋯⋯等都相同。
目前COVID-19全球疫情仍嚴峻,若給對照組的受試者打生理食鹽水的安慰劑、完全沒有保護力,被認為有違倫理。日本「第一三共」(Daiichi Sankyo)日前宣布投入mRNA疫苗「DS-5670a」開發,第三期臨床試驗就不採用照組施打安慰劑的「較優性試驗」(Superiority Trials),而是改採「非劣性試驗」(Non-Inferiority trials),並將與同為mRNA疫苗平台的輝瑞或莫德納(Moderna)對照,是屬第三期臨床試驗。
不過,國產疫苗這次和AZ疫苗的中和抗體比較,因為進行的時間、條件、環境並不相同,以二期臨床試驗做對照、且是跨平台的比較(AZ是腺病毒疫苗、國產疫苗屬蛋白質疫苗),與正規的「非劣性試驗」方式不盡相同。

李建璋(台大臨床醫學教授、急診醫學部主治醫師):
高端疫苗目前做到二期,可以在實驗室裡看到抗體反應,但無法知道病毒真的入侵人體、疫苗能不能真的提供抵抗力。我認為現況來看,若拿高端疫苗來跟已經做到三期期中、國際使用的莫德納、AZ疫苗來一起平行使用,防疫上的風險會比較大。因為真實世界裡,高端疫苗到底保護力效果好不好,目前沒有人知道。
因此,讓高端疫苗作為「補充」使用,是保守穩健的做法。例如,提供給現階段疫苗還不足以涵蓋的族群使用,或是擔心有副作用而不願接種莫德納或AZ疫苗的年長者,作為目前疫苗的補充。
此外,國產疫苗是採次單元蛋白質疫苗,人類使用的歷史悠久,安全性有保障,也不會產生太強烈的免疫反應,反而能保握這優勢,朝另外兩個方向去執行:第一,擴展兒童、青少年試驗,目前mRNA疫苗對年輕族群有心肌炎的威脅,或許可以作為蛋白疫苗的利基。第二,針對年紀大的族群提供疫苗試驗,未來就能針對特定族群,讓國產疫苗扮演一定角色。

黃立民(台大兒童醫院院長、台灣感染症醫學會名譽理事長):
今天高端通過了EUA,接下來最大的難題,就是「如何定位這支疫苗」。應該要當成追加劑?還是都可以全部都適用接種?但專家會議上只有就高端疫苗與AZ疫苗的數據做討論,後續政策上的使用、量能等等,都將由指揮中心及食藥署那邊再去決議。
現在後續的使用方式都還不是很明朗,接下來若直接全面接種國產疫苗,無法明確得知疫苗的保護力如何;若採用追加劑接種,也許還能推估計算保護力,但兩種接種方式,對於保護力的數字都是間接產生的,這是很困難、不太容易解決的問題。
至於審查委員要求附帶條件,是一年內檢送國內外執行疫苗保護效益(effectiveness)報告──這可能會作為未來申請正式藥證時,直接給予許可證的根據,是有這個可能性在的。但未來會不會以這個報告作為許可證依據,決定權還是在指揮中心。

劉宏恩(政大法律學系副教授、衛福部疾管署人體研究倫理審查會委員):
相較於國際上都是三期期中試驗申請緊急授權EUA,台灣在「二期期中試驗」就核准高端疫苗EUA,是世界罕見之舉,食藥署就應對核准的條件做出更多說明。
第一,應只允許高端一段短期核准使用時間,或限期高端在期限內完成三期試驗、申請正式藥證,或比照國外至少完成三期期中分析。目前食藥署並沒有明確說明國產疫苗後續三期試驗的做法,僅附上條件要求「藥商須每月提供安全性監測報告,並於核准後一年內檢送國內外執行疫苗保護效益(effectiveness)報告,以保障國人用藥安全」。但這個保護效益報告又是什麼?審查項目、內容又有哪些?也都沒有清楚告知。
EUA是緊急公衛情事下採用的做法,不是一個長期的使用規範,根據《藥事法》48-2條規定,「當緊急公衛情事已終結」,EUA的專案核准應該要廢止。在法規之下,主管單位食藥署就應該要有機制跟審查標準去評估,這些條件都應該在核准時附上,但這次也沒有附上廢止條件。
第二,標準不應該「滾動式調整」。台灣的臨床試驗在近幾年受到國際肯定,很多國際藥廠都願意來台灣收案,因為台灣的法規、SOP都是透明一致的。但這一次食藥署從去年7、8月開始研擬國產疫苗的作業,很多做法卻採「滾動式調整」,從審查委員名單不公開,到高端公布二期期中分析前8小時、才公告緊急授權核准標準,這些沒有標準的標準,讓生技產業、廠商無所依循,主管機關的公信力也造成傷害,社會各界如今更對於國產疫苗充滿疑惑,「怎麼會沒有標準就滾動?到什麼時候才開始算有標準?」
吳全峰(中央研究院法律學研究所副研究員):
其實EUA的審查資訊要揭露到多少,是沒有明文規定的,但在國產疫苗要核准給民眾使用的狀況下,還是要進行風險溝通,資訊相對愈公開,民眾願意接種疫苗的信賴度就愈高。這次的國產疫苗過程中已經有爭議,今日的新聞稿又只有提出會議幾人投票、幾項條件,但到底專家討論內容、數據如何達標,這些都沒有更多說明、開誠布公細節提供給民眾判斷,無法消弭疑慮,是不好的做法。
此外,指揮中心今宣布,一年後提交「疫苗保護效益報告」,這個「一年」的時間如何計算?指揮中心也沒有說明,假設今天接種人數多,還需要等到一年嗎?同時,今天也沒有公布核准多少數量的國產疫苗,就算沒有明確數字,也應該要有預估數量,否則若在期間內大量製造,並在市面上流通,十分不合理。
其實,台灣的法規上並沒有「緊急授權」、「EUA」這些名詞,我們是採用《藥事法》48-2條,以及子法《特定藥物專案核准製造及輸入辦法》,來專案進口、核准國際疫苗如AZ、莫德納;民間採購如台積電、鴻海遵循的也是這些法條。國產疫苗的核准,照理說也應該遵照相同標準,但目前卻連核准數量都還沒有提供。總之,相關的資訊實在太少,不止讓民眾困惑、專家也都很難評論,主管機關應該要肩負責任,做出更多說明。

黃韻如(台大醫學系教授、防疫科學研究中心國際合作主持人):
台灣食藥署目前是第一個只有二期期中臨床試驗結果、就核給EUA的審查監理單位,這項世界創舉,如果政府真的想要作為引領國際潮流的疫苗審核方式,在專家審查過程沒有留下完整的全程紀錄(錄影或逐字稿),是可惜之處,而對於為何沒有留下完整的全程紀錄的解釋,也令人摸不著頭緒。因為未來起碼可以在簽署雙方保密協定之下,提供審查過程來參考專家評估的嚴謹度,這將有助於台灣未來要與國際主要審核單位的政策接軌。
一般國際接軌還是廠商要根據每一個國家的標準來提供數據,所以高端目前沒有第三期的資料,是無法在其他國家送審的。
而在目前各廠牌外購疫苗已經漸漸補齊的情況之下,國內對於國產疫苗的需求缺口還有多少?民眾對於沒有保護效益資料的國產疫苗接受度到哪裡?都是接下來值得觀察的點。目前食藥署是核准「專案製造」,高端的產能以及交貨期限也考驗著國內廠商的競爭力。
至於這次台灣食藥署採用的免疫橋接方式,雖然普遍認為是未來新一代疫苗可能採行的方式,不過,美國FDA在今年5月的更新指引已經講得很清楚:免疫橋接,是為了現有已通過EUA的疫苗平台所新增的規定,以加快針對變種病毒的下一代候選疫苗發展,不是給還沒有做完第三期臨床試驗、也還沒有拿到EUA的疫苗平台的核准捷徑。
(2021.7.27更新)
7月25日,中央流行疫情指揮中心指揮官、衛福部部長陳時中在記者會中宣布,經過衛生福利部傳染病防治諮詢會預防接種組(ACIP)專家會議討論後,決議可將高端疫苗納入現行的公費接種計畫。
陳時中表示,目前初步會建議將高端疫苗提供給對腺病毒(AZ疫苗)、mRNA(莫德納疫苗)過敏、不適合的族群優先使用,其他使用狀況,還是會由指揮中心再根據疫苗施打狀況做規劃。
7月27日,指揮中心則宣布,將重新開放公費疫苗預約平台,高端疫苗也列入意願登記的疫苗之一,提供給20歲以上的民眾,但接種時間還不明確,得看整體供應量的情況。
至於高端疫苗何時應完成三期,或至少做完三期期中分析,以及一年後要提交的疫苗保護效益報告,目前指揮中心都還沒有詳細說明時程,陳時中表示,這部分仍會由食藥署負責監管。
深度求真 眾聲同行
獨立的精神,是自由思想的條件。獨立的媒體,才能守護公共領域,讓自由的討論和真相浮現。
在艱困的媒體環境,《報導者》堅持以非營利組織的模式投入公共領域的調查與深度報導。我們透過讀者的贊助支持來營運,不仰賴商業廣告置入,在獨立自主的前提下,穿梭在各項重要公共議題中。
今年是《報導者》成立十週年,請支持我們持續追蹤國內外新聞事件的真相,度過下一個十年的挑戰。