聯亞、高端兩支國產疫苗擴大二期臨床試驗相繼解盲,繼高端二期臨床達標後,聯亞今(6月27日)也公布,二期報告分析結果。但2支疫苗仍將與英國AZ疫苗進行免疫橋接PK,得證明中和抗體效價不比AZ疫苗差才能達到食藥署自訂的「國產COVID-19疫苗緊急使用授權(EUA)審查」保護力標準。
然而,國產疫苗要到達讓國人接種的目標,還有兩大難題:審查公信和量產能力。近日EUA審查會議與委員名單遭外界質疑有人球員兼裁判,《報導者》掌握到,一篇國產疫苗研究成果的國際論文中,疫苗業者與審查專家共同掛名作者,出現利益衝突。而即便解決種種審查過程的爭議,業者成功獲EUA授權,我們獨家取得兩家業者與疾管署預訂採購各500萬劑的合約發現,兩家業者交貨期程極長,聯亞分4批到11月底才需完成交貨、高端則分5批可到12月中才交貨。除了疫苗效果評估,其實,量產能力更是國產疫苗產業脆弱的阿基里斯腱。
聯亞生技今公布疫苗擴大二期的期中報告分析,3,850位受試者分成12~18歲青少年、19~64歲成年人及65歲年長者三個族群,在今年2月26日~5月18日完成兩劑接種,6月下旬將所有原始資料委託第三方臨床試驗受託機構進行數據彙整顯示,抗體效價在疫苗接種第二劑後28天的血清陽轉率,成年族群為95.65%、老年族群為88.57%,中和抗體效價為102.3;也未出現嚴重不良反應。不過,與高端公布的內容一樣,沒有詳細的指標,血清陽轉率僅代表與未接種疫苗的人比較,出現的抗體反應比率,無法等同疫苗保護力。
聯亞董事長特助彭文君表示,這支疫苗對目前各種變種病毒株如英國Alpha、南非Beta、巴西Gamma、印度Delta的中和抗體沒有下降太多,尤其對目前全球流行的Delta變種病毒株,中和抗體效價也維持同一水平。但他強調,這份報告和高端一樣,皆屬「二期期中分析」,真正解盲要到11月才完成。聯亞生技行政管理中心副總經理暨發言人范瀛云說,6月底會向食藥署繳交期中分析報告及技術文件,申請EUA緊急授權;同時宣布,三期臨床試驗將在印度進行,規模為11,000人。
彭文君解釋,針對變種病毒株的實驗,是使用臨床一期受試者血清的中和抗體,對不同變種病毒株來進行測試。長庚大學新興病毒感染研究中心主任施信如說,這無法直接推論疫苗就對變種病毒株有效,中間還有很多問題需要克服,「不過其實目前全球試驗看來,Delta病毒株雖然傳染力高,但本來疫苗效力就能維持,不像巴西、南非株有明顯降低的情況。」
施信如表示,由於不同實驗室做出的中和抗體數據會差非常多,因此這次兩家疫苗廠的數據,都是由中研院做出來,才能相互比較。「關鍵是在聯亞的中和抗體效價只有102.3,跟高端600多比起來,就算有保護力,保護效果也很低。」(延伸閱讀:〈緊急授權標準最後一刻出爐,高端二期成功、聯亞月底揭曉,但得和AZ做療效PK〉)
施信如表示,未來兩支疫苗都要跟AZ疫苗PK,AZ疫苗全世界已經打了上億劑,其中和抗體已經可以推算出國際標準單位,台灣也可以自己換算;目前換算看起來,AZ跟高端的數值都在600多,但若同樣方式換莫德納(Moderna)則是2000多,「而且,台灣的AZ資料就200人,值就會偏低,這樣國際上怎麼解釋我們如何研發、通過疫苗?」
不過,聯亞疫苗較特殊的部分,是同時分析出疫苗能產生T細胞免疫反應,誘發殺手T細胞殺死被病毒感染的細胞,有助於預防重症,是中和抗體以外的保護力指標,施信如說,「看起來效果很可能不錯,可是T細胞的效果沒辦法從中和抗體判斷,只能做三期臨床試驗才會知道結果。」
兩家業者能否取得EUA,仍需先經過預計在7月中進行的新冠肺炎疫苗臨床試驗專家會議審查,由專家投票後供食藥署做為最後是否給予EUA的決策參考。儘管專家會議審查小組為諮議性質,但按國際慣例,投票結果多半具有極大影響力,委員的資格與利益迴避問題也受到重視,但卻在台灣爭議不斷。
食藥署和醫藥品查驗中心(CDE)自訂全球第一個COVID-19疫苗的「免疫橋接」標準,取代國際三期臨床研究方式做為保護力指標,因評估標準未與國際同步,專業界看法迄今嚴重分歧、爭辯未止。連日又爆出EUA相關專家委員名單疑為特定立場布樁的風波,食藥署緊急發布新聞滅火,強調專家會議依不同議題邀請不同專家,而委員均須簽署利益迴避及保密同意書。
不過,關鍵的5月6日確立免疫橋接做指標及28日確立橋接比較標準會議中,列席專家的中研院生醫所研究員林宜玲,其實驗室不僅為此次國產疫苗臨床試驗解盲前進行血清中和抗體檢測,也同時負責國產疫苗與AZ進行PK的免疫橋接的中和抗體效價比對任務。由於國產疫苗保護力是否合格,必須和3月部立桃園醫院200名接種AZ疫苗者的中和抗體進行比較,兩者確實必須在同樣實驗室標準與環境進行,無法切分;但在關乎可否取得EUA的關鍵檢測工作中擔任要角,是否合適聘為官方專家委員,即已引發球員兼裁判的質疑。
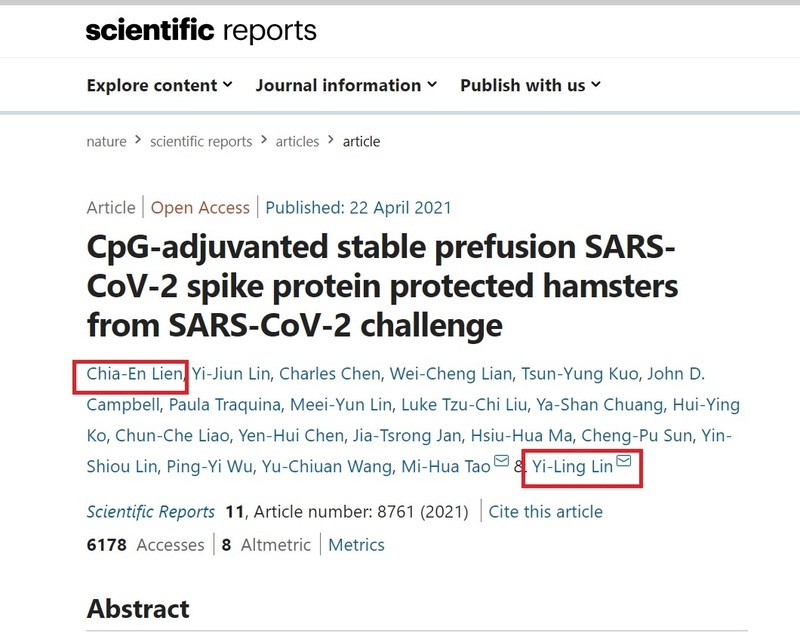
《報導者》則掌握,高端疫苗日前發表的一篇國際期刊,林宜玲列名最重要的「通訊作者」,已是高端疫苗相關研究的「直接參與人」。4月21日英國《科學報告》(Scientific Reports)期刊上一篇論文上,刊登高端疫苗的相關研究,證明在倉鼠動物模型中,其疫苗使用的CpG 佐劑可維持疫苗穩定,增強免疫抗原反應,保護倉鼠避免病毒攻擊。而該篇論文中,第一作者是高端疫苗生物製劑公司國際暨公共事務處處長連加恩、通訊作者即為林宜玲。
正式國際期刊上,相關研究依貢獻度而掛名,其中,最重要的就是通訊作者(corresponding author)和第一作者(first author)。 通訊作者雖然是列在作者名單中的最後一位,一般就是代表整個「研究計畫的主持人」,需對論文負最大部分的責任;第一作者則是列在作者名單上的第一個人,是實際從事大部分實驗與分析工作的人。
林宜玲透過中研院院方回應表示,「首先我不負責任何疫苗公司的解盲,我也不是任何一家疫苗公司EUA的審查委員,對於論文發表,一向秉持open science,與大家分享的精神,不管是學研界或是廠商,都尊重委託方的意願。」中研院則表示:「對此沒有任何回應。」
食藥署藥品組科長黃玫甄表示,事前就已經知道林宜玲在中研院負責此次國產疫苗臨床試驗解盲前進行血清中和抗體檢測一事,但因為會議是討論原則性問題,並非針對特定廠商,如果是特定廠商的審查案件,就需要迴避,「我們(食藥署)本來就知道她有幫忙(檢測中和抗體),因為台灣的P3實驗室很少,能夠做的專家沒有幾個,但因為會議是原則問題討論,所以認定沒有利益衝突。」
不過,黃玫甄表示,食藥署沒有掌握林宜玲與高端共同發表論文這件事情,但她表示會議沒有討論個別案件,因此同樣沒有利益衝突,「邀請林宜玲參與會議的目的,是希望她針對過去實驗室如何進行中和抗體做說明,提供在場專家了解檢測與分析方式。」
食藥署聲稱EUA的委員都有進行利益迴避,標準設在哪?流程又是什麼?長年在疾管署人體研究倫理審查會及醫院、藥品審查人體試驗委員會(IRB)等擔任審查工作的政治大學法律學系副教授劉宏恩說,「所有的審查制度就是在建立『公信力』,利益迴避的標準是主管單位要明確訂出來的,不是交由專家自由心證,從沒看過像這次COVID-19疫苗審查會議和委員利益迴避這麼『混沌』的一次。」
劉宏恩舉例,在一般審查作業,很明確會有三個階段:建立利益迴避的標準、過濾專家背景、最後才由專家自己確認後簽名,「以科技部研究計畫申請,利益迴避的標準包括,審查委員不能與申請者曾經有共同執行計畫、不能曾為指導教授和學生關係等等,很明確條列出來。要不然全交專家自己認定,大家認知不同,反而是陷專家於不義。」
台大醫院臨床試驗中心主任陳建煒表示,自己是在今年3月後才獲邀參與這次疫苗相關審查會議,第一次是審莫德納(Moderna)的EUA,「但因為我的小孩在莫德納工作,我便迴避了那次會議。」另一名國產疫苗臨床試驗的負責人則對我們透露,「後來也是我自己覺得工作和專家身分有衝突,主動婉拒了後續的會議邀約。」
「食藥署解釋,不同會議與會專家不同,但從去年(2020)10月定出擴大二期、3,000人初步標準,到後來採免疫橋接、和AZ進行PK,這些會議看來都是要訂出EUA標準,應有其一貫性,這樣的說法無法回應大家的疑慮,」劉宏恩並提到,美國的EUA審查流程,在專家訂出標準不代表就定案,會公告後開放接受各界意見,然後彙整討論進行調整,所以有時會有一版、二版,「台灣這次會引起那麼大風波,就是從去年10月起,EUA標準怎麼訂出來?一路都不夠開誠布公,讓懷疑的人更懷疑。反而讓參與的專家一併被連累。」
疫苗在實驗室裡實證,但不是在實驗室裡就能「完成」。疫苗生產真正最困難的在於「量產」,擴大產能後是否能讓疫苗穩定及有足夠的原物料,才是疫苗產業最大的考驗。
連日來在美國、日本和立陶宛捐贈下,目前台灣已到貨587萬多劑有國際認證的AZ和莫德納疫苗;不過,距指揮中心之前估計60%群體保護需要的3千萬劑,尚有一段距離。國產疫苗若在解決審查公信力以及成功達到目前訂出的標準後,要立即上場救援,量產能力仍是問號。
我們獨家取得的疾管署和兩家國產疫苗簽訂各500萬劑的預購合約草案,高端和聯亞若取得EUA,第一次交貨期程是8月底,高端只需交40萬劑、聯亞則是90萬劑;整個交貨期程拉到年底,高端分5批、最後一批是12月15日,聯亞分4批、到11月30日。也就是,在台灣社區疫情尚未能控制,傳播速率比目前主流的Alpha變種病毒可能高1倍的Delta變種病毒又已入侵之下,8月前兩家業者僅需交130萬劑的數量,難以發揮巨大作用。
已向食藥署遞交EUA申請的高端,不僅要面對COVID-19疫苗可能趕製的狀況,日前還宣布腸病毒71型疫苗三期試驗有效性良好,將申請藥證,也在生產線上。高端疫苗副總暨發言人李思賢表示,高端的竹北廠有兩條產線,目前規劃一條生產腸病毒疫苗、一條生產蛋白質原液(即COVID-19疫苗),雖然兩種疫苗的平台不同,前者為滅活病毒、後者為次單位蛋白疫苗,但生產線只要清消後就能轉換。意即只要EUA通過,高端生產線會全部集中產製COVID-19疫苗。
范瀛云則表示,聯亞原本就是生產蛋白質原液和疫苗充填廠起家,2013年切分出兩家子公司聯合生物製藥(聯生藥)和聯亞藥業(聯亞藥)負責生產和填充,2014年買下GSK (荷商葛蘭素史克藥廠,GlaxoSmithKline)亦有針劑廠。「GSK這個廠房是國際標準GMP(Good Manufacturing Practice,藥品優良製造作業規範)廠房,無菌針劑產線也同時通過美國FDA與日本厚生省PMDA查廠過,今年底還會再進新的生產機台,如果全力衝刺,一年可以有一億劑產量、明年擴充生產線可以到4億。」
長庚大學臨床醫學研究所副教授顧正崙解釋,包括高端和聯亞,目前都以蛋白質疫苗為主,「蛋白質疫苗量產,最重要的關鍵就在蛋白質原液和充填。蛋白質純化過程浸泡在不同的溶液中會不會造成改變?也是放大製程中品質穩定度的考驗。所以,蛋白質疫苗雖然相較這次的全新的mRNA和腺病毒疫苗,使用的經驗較多,但從開發到能夠穩定量產,一年是合理的時間。」
要讓國產疫苗上路,包括經濟部、生技中心等,都在盤點資源。一名官員透露,「蛋白質發酵反應不是等倍計算,200公升發酵成品就會等於4倍的50公斤,像高端是全蛋白疫苗、形狀像三葉草,發酵後一定要長出那個形狀,很多蛋白質疫苗容易在放大的過程中失真,就無法引發特定抗原而無效、甚至可能引發其他副作用。高端本來只有50公升的蛋白質發酵反應器,放大到200公升時還可以,但到1,000公升後就有瓶頸,所以委外給台灣目前最大的蛋白質原液工廠台康代工。」

一支疫苗,從找到有效的標的,用臨床試驗證明安全性和有效性,其實能否取得核可,量產能力也是考量。和國產疫苗同為蛋白質疫苗的諾瓦瓦克斯(Novavax),公布的保護力效果極佳,也面臨量產問題,未來得及申請美國EUA、只能在今年第三季直接申請藥證。
檢視高端和聯亞的產程,「高端部分疫苗標的物、佐劑,是由美國授權或採購,原液、針劑、充填則幾乎是外包,比較缺乏的是核心技術;聯亞的原料和充填廠是自己供應,但關鍵的疫苗如何調製比較神祕,至今沒有公開,很難評斷,」顧正崙說。
聯亞在疫苗部分,過去未涉足人用疫苗,只有動物疫苗的經驗,O型口蹄疫合成胜肽疫苗在中國上巿;疫豬隻免疫去勢疫苗則是在俄羅斯和中南美洲上巿。「這家公司過去是熱門的開發項目都會參與,但完成的成果很少,」一名經濟部官員私下表示。
疫苗解盲前夕,聯亞子公司聯亞藥因為興櫃價格由30元狂飆到300元,金管會表示櫃買中心將依法查核注意。而旗下另一聯生藥,其實也曾於2014年9月登錄興櫃,但在2018年8月撤櫃。
「若全面盤點台灣蛋白質原液工廠,台康、聯亞、藥華大約都有12個2,000公升的蛋白質反應器發酵糟,再加上其他小廠,全面啟動的話,可以到6萬到7萬升的量,」生物技術開發中心執行長吳忠勳指出,「但是,大家可能很難想像,其實一個疫苗需要的原料還有很多,像是發酵槽的無菌包膜塑膠袋,這個全世界沒有幾家工廠生產,疫苗開發時,大家都在搶這個,叫貨時間長達9個月到1年之久。」
此外安瓶、針劑等雖然技術難度不高,也是疫苗產線的關鍵原料,有些工廠過去在台灣利潤不高,已出走台灣;甚至連原液廠,也有的在巿場考量下移轉到中國。日商新藥開發平台Gemseki亞洲地區部長宋豪麟指出,「中國因為要求生物藥只能用中國自產,有些台灣業者為了要訂單,只能轉到中國設廠。我先前為了替一支新藥在台灣找蛋白質原液代工的報價,結果除了台康,找不到第二家報價。」
宋豪麟說,1公升的蛋白質反應器只能產出4克蛋白質疫苗,「在韓國,他們目前光疫苗代工廠,有13個1萬升的反應器。」
美國去年5月成立的「神速行動小組」(Operation Warp Speed),即由衛生部與國防部共同籌組,重點就是在加速新冠病毒疫苗研發、製造與配送的流程,確保今年1月前開始施打疫苗,預算高達180億美元(逾新台幣5千億元)。不過,輝瑞(Pfizer)藥廠一開始並未申請補助,但也在冷鏈技術和原物料需求卡關,美國為了保證「取得足夠的疫苗數量」,進一步通過《國防生產法》,掌控疫苗關鍵的脂質、無菌袋等原物料,提供廠商生產必要的協助,輝瑞才加入「神速行動小組」中。
近日國產與國際疫苗價格訂價也引發熱議。莫德納每劑在25~37美元間(約新台幣690~1,021元)、AZ疫苗則在2.15~5.25美元間(約新台幣59~145元),輝瑞為19.5美元(約新台幣538元)、諾瓦瓦克特(Novavax)16美元(約新台幣442元)、嬌生(Johnson & Johnson)為10美元(約新台幣276元);國產疫苗目前採購價格,高端為881元、聯亞為750元,許多人也解讀,國產量能少、價格就會偏高,同時也反映,前期投資太少。
但若與2009年H1N1新流感疫情相較,這次COVID-19的採購條件已大躍進。當年台灣首次因應緊急疫情自行開發疫苗,完成國產疫苗開發的國光生技董事長詹啟賢對我們證實,「那時囿於《政府採購法》,政府仍是先招國際標,2次流標後才進行國際、國內混合招標,國光得標的價格是199元,比常規流感疫苗110元稍高一點。而且8月議約、10月要交貨,合約第一條,廠商要先繳給政府10%的履約保證;交貨延遲,慢一天罰總價金的5%。」但他也強調,H1N1流感疫苗只是在原本季節性流感置換H1N1病毒株進行生產,和這次COVID-19從頭研發、要證明安全性和有效性有所不同。
這次政府投資雖無法與歐美投資規模相比,但也編了135 億的國產疫苗研發經費,補助近一半;進入臨床試驗不同階段,也有目標獎金,最高可再拿5億,這些是在採購之外的補助。而疾管署與兩家國產廠商採購合約中註明,「已盡商業上最大努力而仍無法履約者,機關同意不對廠商追債已支付的契約價金」,也已是史上首見。當然,這份採購契約只是訂單,若最後2家業者EUA申請失敗,採購等同失效。
前疾病管制局(現為署)局長、現數位防疫產業大聯盟召集人張鴻仁指出,疫苗是賣給政府,是低利潤、高風險的行業,多數業者都會選擇投資容易賺錢的新藥、新醫材,疫苗就成了相對低投資的領域。多數如台灣人口規模的國家,甚至沒有疫苗的自製能力,台灣目前有3家疫苗廠、有產業鏈,但過去卻一直沒有積極發展國內的疫苗,「反正市面價格很低,買就好了,」導致國產疫苗佔比不到10%。
未來應該要把握機會,把國內自主供應鏈建立起來。張鴻仁認為,第一要修改《政府採購法》,讓採購更彈性。這次不少批評「國產疫苗還沒成功,指揮中心就採購」的聲音,未來若要做好準備,就應該讓採購更彈性,政府得以採購還在臨床試驗中、不確定會不會成功、何時能交貨的產品,不會被定義成圖利廠商。第二要訂定中長程的5年目標,提高國產疫苗使用比例達50%,國內的疫苗思維,應該要從進口替代,慢慢將一半轉為自製、累積實力後最終外銷出口。
第三,投資新技術。全世界有幾十家mRNA平台公司,中國就佔了三分之一,台灣一家都沒有。疫苗產業規模約莫幾十億元,國家是可以投資的。國光、聯亞國發基金曾經投資、高端則是民間自立。整體來說,過去國家注入低、訂單不多、研發補助也不夠穩定。
但要發展疫苗產業,也無法自己關起門來做,台灣要進入國際的正規賽程中,必須把疫苗產業和防疫分開來考量。陳建煒便強調,「疫苗開發無論成功或失敗,最重要的是走在『對的流程』,才能持續累積實力,每一步都關乎台灣的『國際品牌』和形象,這次在EUA的標準、審查會議的種種爭議,如果不導正,會給台灣生技發展帶來創傷。整體大眾如果對於國內生技發展只看成金錢遊戲,社會會走偏,那是不成熟、不健康的。」
劉宏恩也提到,國際標準不僅是疫苗評估的標準,也包括法規的國際化,「以臨床試驗為例,過去5、6年台灣逐步建立起國際認證單位,我們一天到晚和醫療人員、藥廠業者宣導和建立程序,試驗中不能對外放消息。結果這次卻是政府帶頭,先是衛福部公開替業者召募臨床試驗者、後來明示暗示『樂觀期許』、何時可望打到疫苗,都是近年新藥臨床試驗不會發生的事,這次全部發生,會破壞台灣法律環境的基礎。」他指出,「國際藥廠要尋找臨床試驗的合作地區,不是貪圖你的法律寬鬆、進行方便,而是這個地方做出來的結果和品質,是否是值得信賴。」
國產疫苗二期解盲後是否能獲EUA授權,不應視為這次國產疫苗的「結果」,其實只是一個開端,我們需要不斷校正回歸的是,如何在變動的環境之下,過程與決策在正確與可行的方向。
深度求真 眾聲同行
獨立的精神,是自由思想的條件。獨立的媒體,才能守護公共領域,讓自由的討論和真相浮現。
在艱困的媒體環境,《報導者》堅持以非營利組織的模式投入公共領域的調查與深度報導。我們透過讀者的贊助支持來營運,不仰賴商業廣告置入,在獨立自主的前提下,穿梭在各項重要公共議題中。
今年是《報導者》成立十週年,請支持我們持續追蹤國內外新聞事件的真相,度過下一個十年的挑戰。